小分子“重写”细胞命运:温医大附属眼视光医院苏建忠/瞿佳团队联合高绍荣院士团队实现视网膜色素上皮细胞化学重编程修复视功能
近日,视觉健康全国重点实验室、温州医科大学附属眼视光医院苏建忠/瞿佳团队联合同济大学高绍荣院士团队在Nature Communications(IF 15.7, 中科院1区)发表题为“Chemical reprogramming of fibroblasts into retinal pigment epithelium cells for vision restoration”的研究论文。研究提出一条完全依赖小分子化合物、无需基因编辑的两阶段化学重编程策略,可将成纤维细胞高效诱导为结构与功能均接近原代细胞的视网膜色素上皮(RPE)细胞,并在视网膜变性模型中改善视觉功能,为退行性视网膜疾病提供了安全、可控、具规模化潜力的新型细胞来源。

研究背景
年龄相关性黄斑变性(AMD)和视网膜色素变性(RP)等视网膜变性疾病是全球致盲的主要原因之一,一旦RPE细胞受损,视力往往难以逆转性恢复。尽管细胞替代疗法前景广阔,但如何获得安全、稳定、可大规模制备的 RPE 细胞仍是再生医学领域的关键挑战。
研究亮点
研究团队自主建立了基于单细胞的重编程化合物筛选平台scRCF(single-cell Reprogramming Compound Finder),系统整合单细胞转录组、药物靶点数据库及转录因子—小分子调控网络,通过算法预测可推动“去纤维化—去分化—眼场化—RPE定向”连续转变的关键节点,并结合 DRUG-seq2高通量表达谱筛选,大幅提升了小分子组合设计的效率与准确性。
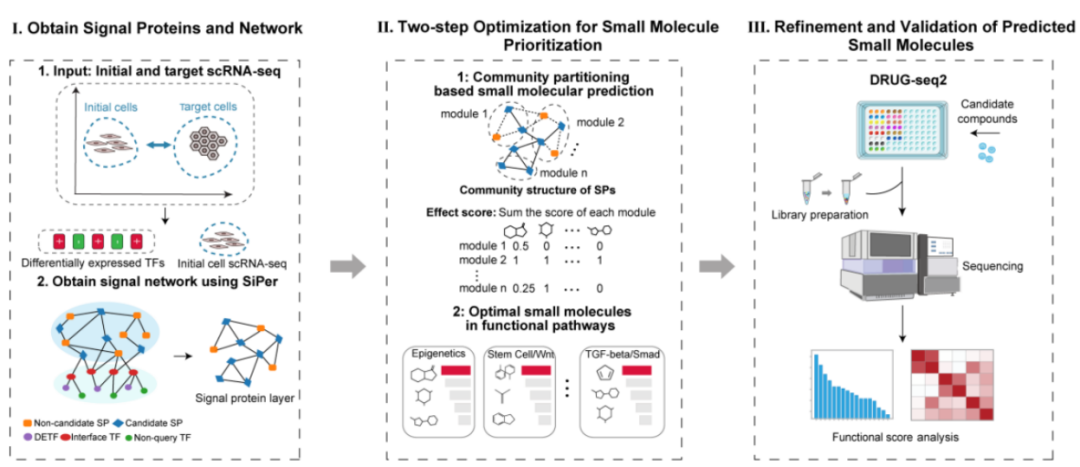
在scRCF的指导下,团队构建了完全由小分子驱动的“两阶段化学重编程体系”,成功实现了鼠源与人源成纤维细胞向RPE细胞的诱导(ciRPE)。ciRPE在形态、超微结构及分子特征上与原代RPE高度一致,具备吞噬外节、形成高跨上皮电阻屏障和极性分泌等关键功能,并表现出良好的扩增能力与染色体稳定性,具备面向规模化制备的潜力。
多组学分析揭示了重编程过程中转录因子级联与表观遗传重塑的关键调控逻辑,其中Ascl1、Olig2及眼场发育相关因子在命运决定中发挥核心作用。体内研究显示,ciRPE能在RCS模型大鼠中稳定整合于宿主RPE层,改善感光细胞存活并提升视觉功能,且未见肿瘤形成,证明其具有良好的生物相容性与应用前景。
研究意义
该研究建立了首个完全由小分子化合物驱动的RPE化学重编程体系,为获得安全、可规模化制备的RPE细胞提供了新的解决路径。多组学分析阐明了命运跨越的关键调控机制,深化了对RPE生成与视网膜再生生物学的理解。体内实验验证其良好整合能力与视觉功能改善,显示出应用于AMD等退行性视网膜疾病的现实转化潜力,为未来发展自体化、标准化的细胞替代治疗奠定坚实基础。
温医大附属眼视光医院学术院长苏建忠教授,同济大学生命科学与技术学院院长高邵荣教授及温医大附属眼视光医院终身名誉院长瞿佳教授为本研究的共同通讯作者。温医大附属眼视光医院与瓯江实验室联合培养博士后李莎莎、温医大附属眼视光医院刘慧副研究员和潘少辉副研究员为本研究的共同第一作者。 原文链接:
https://www.nature.com/articles/s41467-025-67104-w